1, 2-விட்டிக் மறுசீராக்கல் வினை
1, 2-விட்டிக் மறுசீராக்கல் வினை (1,2-Wittig rearrangement) என்பது ஈதருடன் ஆல்கைல் இலித்தியம் சேர்மம் வினைபுரியும்போது ஈதரில் நிகழ்கின்ற 1,2-மறுசீரமைப்பைக் குறிக்கிறது. கரிம வேதியியலில் நடைபெறுகின்ற வகைப்படுத்தப்பட்ட வினைகளில் மறுசீராக்கல் வினை என்பதும் ஒரு வினை வகையாகும்[1][2]. நோபல் பரிசு பெற்ற வேதியியலாளர் கியார்க் விட்டிக் என்பவர் பெயரால் இவ்வினை அழைக்கப்படுகிறது.
- [math]\displaystyle{ \mathsf{ R'{-}\!\!\!\!\overset{\displaystyle H \atop \vert }{\underset{ \vert \atop \displaystyle \ \ R''}{C} }\!\!\!\!{-}O{-}R + {\color{Gray}{R'''{-}Li} } \ \longrightarrow \ R'{-}\!\!\!\!\overset{\displaystyle R \atop \vert }{\underset{ \vert \atop \displaystyle \ \ R''}{C} }\!\!\!\!{-}O{-}Li + {\color{Gray}{R'''{-}H} } \ \xrightarrow{\displaystyle H^+} \ R'{-}\!\!\!\!\overset{\displaystyle R \atop \vert }{\underset{ \vert \atop \displaystyle \ \ R''}{C} }\!\!\!\!{-}O{-}H } }[/math]
ஆல்காக்சி இலித்தியம் உப்பு ஓர் இடைநிலை விளைபொருளாகவும் ஓர் ஆல்ககால் இறுதி விளைபொருளாகவும் கிடைக்கின்றன. R" என்பது சயனைடு குழுவைப் போல ஒரு நல்ல விடுபடும் குழுவாகவும் எலக்ட்ரானை எடுத்துக் கொள்ளும் வேதி வினைக்குழுவாகவும் இருந்தால் இவ்வினை நிகழ்கிறது[3] இக்குழுவானது நீக்கப்பட்டு தொடர்புடைய ஒரு கீட்டோன் உருவாகிறது.
- [math]\displaystyle{ \mathsf{ R'{-}\!\!\!\!\overset{\displaystyle H \atop \vert}{\underset{\vert \atop \displaystyle \ \ CN}{C} }\!\!\!\!{-}O{-}R + {\color{Gray}{R'''{-}Li} } \ \longrightarrow \ \overset{\displaystyle O \atop \vert\vert}{\underset{\diagup \ \diagdown \atop \displaystyle R'\ \ \ R}{C} } + {\color{Gray}{R'''{-}H} } + LiCN } }[/math]
வினை வழிமுறை
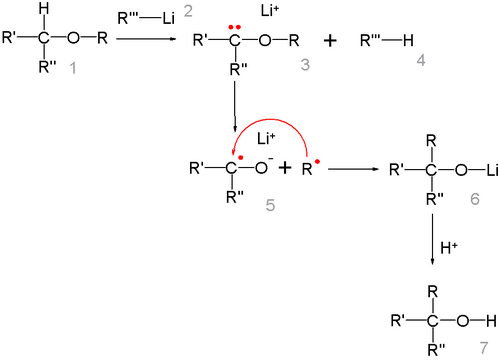
இலித்தியத்துடன் கூடிய ஒரு தனி உறுப்பு இணை கார்பன் அணுவிலிருந்து ஆக்சிசன் அணுவிற்கு இடம்பெயர்வதை மையமாகக் கொண்டே வினைவழி முறை அமைகிறது. R தனி உறுப்பு பின்னர் மீண்டும் கீட்டைலுடன் சேர்கிறது.[4]
.
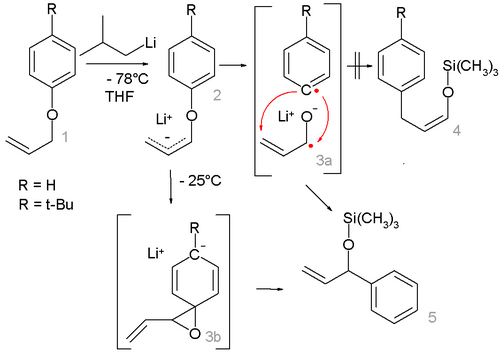
வெப்ப இயக்கவியல் நிலைப்புத்தன்மை அடிப்படை வரிசையில் ஆல்கைல் குழு இடம்பெயர்கிறது. மெத்தில் < முதலாம் நிலை ஆல்கைல் < இரண்டாம் நிலை ஆல்கைல் < மூன்றாம் நிலை ஆல்கைல் என்ற வரிசையில் தனி உறுப்பு வழிமுறை அமைகிறது. கரைப்பான் கூடு விளைவு காரணமாக தனி உறுப்பு-கீட்டைல் இணை சிறிது நேரத்தில் சில மாற்றியமாதல் வினைகள் நிகழ்கின்றன. எலக்ட்ரான் அமைப்பு தலைகீழ் திருப்பமாக மாறுகிறது. சில அல்லைல் அரைல் ஈதர்களுடன் வினை என்றால் இணை வினை வழிமுறை நிகழ்கிறது[4]. −78 °செல்சியசு வெப்பநிலையில் அல்லைல்பீனைல் ஈதரின் வினை 1 இலித்தியமேற்ற இடைநிலையைக் கொடுக்கிறது. 2 இதை −25 °செல்சியசு வெப்பநிலைக்குச் சூடுபடுத்தும் போது மட்டும் மறுசீராக்கல் விளைபொருளாக 5 மாறுகிறது. ஆனால் இலித்தியம் ஆல்காக்சைடுடன் டிரைமெத்தில்சிலில் குளோரைடு கவர்ந்து கொண்ட பின்னர் மாறுவதில்லை. இதனால் மெய்செனெய்மர் அணைவுச் சேர்மத்திற்கு 3b ஆதரவாக தனி உறுப்பு-கீட்டைல் இடைநிலை3a வெளியேற்றப்படுகிறது. ஒரு பாரா-மூன்றாம் நிலை-பியூட்டைல் பதிலீட்டுடன் வினை செயலிழந்திருப்பதைக் கண்டுபிடிப்பதன் மூலம் இந்த வினைவழிமுறைக்கான கூடுதல் சான்று கிடைக்கிறது.
இவ்வினை ஒரு மரபுசார்ந்த டையோடிராபிக் வினை வகையாகும்.
மேற்கோள்கள்
- ↑ Georg Wittig, L. Löhmann, Ann. 550, 260 (1942)
- ↑ G. Wittig, Experientia 14, 389 (1958).
- ↑ Preparation of aryl benzyl ketones by [1,2]-Wittig rearrangement Alan R. Katritzky, Yuming Zhang, Sandeep K. Singh Arkivoc pp. 146–50 2002 (vii) link
- ↑ 4.0 4.1 Wittig Rearrangement of Lithiated Allyl Aryl Ethers: A Mechanistic Study Sven Strunk, Manfred Schlosser European Journal of Organic Chemistry Volume 2006, Issue 19 , pp. 4393–97 எஆசு:10.1002/ejoc.200600304